
2023年的科学突破奖和引文桂冠奖都授予了在CAR-T细胞疗法中作为开创性工作的 Carl June教授和Michel Sadelain教授,这也让他们成为热门的诺奖候选人。
在纪念斯隆凯特琳癌症中心工作期间,Michel Sadelain开发了一种新方法,使用病毒载体对人类T细胞进行基因重组,让T细胞表达出特定的抗原受体,从而靶向癌细胞。这些研究为后来的CAR-T细胞疗法奠定了基础。
2012年,Carl June团队使用CAR-T细胞疗法成功治愈了一位名为Emily的急性白血病复发的小女孩。2017年,FDA批准了第一款CAR-T细胞疗法上市,如今,已有6款CAR-T细胞疗法获得FDA批准上市,还有数百项正在进行临床试验。
CAR-T细胞疗法是一种所谓的“活细胞药物”,是把病人的T细胞在体外通过生物工程改造,使其识别肿瘤细胞表面的抗原,然后把这些细胞输回病人体内,达到识别、杀死癌细胞的效果。CAR-T细胞疗法的出现改变了癌症治疗格局,在血液肿瘤中展现出传统疗法无可比拟的治疗效果。
2023年11月7日,纪念斯隆凯特琳癌症中心的Michel Sadelain团队在癌症领域顶刊 Cancer Discovery 上发表了题为“Disruption of SUV39H1-mediated H3K9 methylation sustains CAR T cell function ”的研究论文。
这项研究表明,只需破坏CAR-T细胞中的单个基因——SUV39H1,就足以让CAR-T细胞更强大,促进CAR-T细胞扩增,防止其耗竭,帮助它们更长时间地对抗肿瘤,防止肿瘤复发。这也提示了我们,CAR-T细胞的表观遗传编程具有平衡其功能和持久性的潜力,可用于改善过继细胞疗法。
论文共同第一作者Nayan Jain博士表示,如果可以通过破坏单个基因来帮助CAR-T细胞维持其功能,这将带来广泛的治疗益处。许多癌症患者在接受CAR-T细胞治疗之前已经接受了多种化疗,这导致他们的T细胞被耗尽,因此难以增殖和有效地对抗癌症。而这项研究开发的新方法只需要更少的CAR-T细胞,可以扩大符合这种治疗条件的癌症患者群体,还还可以提高对患者的治疗效果。
论文共同第一作者赵泽国博士表示,通过这种新方法,在延长CAR-T细胞寿命的同时,还能保持其肿瘤杀伤能力,因此我们可以使用更低的剂量来治疗患者,这可能会减少细胞因子释放综合征(CRS)的出现。
在治疗过程中,CAR-T细胞会随着时间的推移而失去功能,这种被称为T细胞耗竭(T cell exhaustion)的现象,一直是CAR-T细胞治疗面临的主要障碍。这会导致CAR-T细胞在短期内有效。
30年前,Michel Sadelain 教授首次设计了T细胞,并一直致力于改进CAR-T细胞。他和团队的早期研究表明,当T细胞中的某些基因被关闭时,T细胞会随即发生耗竭,是什么关闭了这些基因?答案是——细胞的表观遗传学。
我们可以把表观遗传学比喻成DNA上的调光开关,调光开关在不改变灯具的情况下改变灯光亮度。同样的,表观遗传学可以在不改变DNA序列的情况下,改变基因表达水平。
许多表观遗传学变化的发生是由于DNA在细胞核中的包装方式。在染色体中,DNA双链被称为组蛋白的蛋白质包裹着,在DNA和蛋白质紧密包装的区域,基因是不可访问的,也无法启动表达。
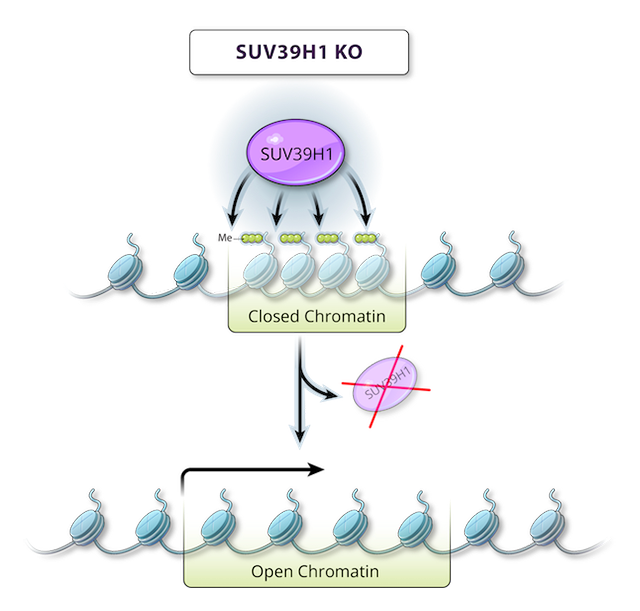
SUV39H1是一种H3K9甲基转移酶,介导H3K9甲基化,从而抑制多个基因的表达。研究团队认为,与其试图改变所有这些被抑制的基因的表达,不如专注于破坏SUV39H1,从而同时微调被其抑制的多个基因的表达,以增强T细胞功能。
研究团队使用CRISPR-Cas9基因编辑技术敲除了人类CAR-T细胞中的SUV39H1基因,然后将这些基因编辑过的CAR-T细胞输入移植了人类白血病细胞或前列腺癌细胞的小鼠体内。结果显示,对于这两种癌症,基因编辑过的CAR-T细胞能够维持它们的功能而不会耗竭,从而导致肿瘤的完全消除。相比之下,未经基因编辑的CAR-T细胞治疗的肿瘤小鼠模型未能存活。
此外,为了验证基因编辑过的CAR-T细胞的持久性,研究团队将治疗后的小鼠暴露于新的肿瘤,结果显示,敲除SUV39H1基因的CAR-T细胞能够防止肿瘤复发。
这项在小鼠模型上进行的临床前研究证明了敲除SUV39H1基因的CAR-T细胞不仅具有更强、更持久的抗肿瘤效果,而且未发现严重副作用。此外,研究团队已将该技术授权给了生物技术公司Mnemo Therapeutics,以推进基于这项研究的临床试验。